Bioquímica UFPR
Este blog foi criado pela profa Silvia Prado para postagens de assuntos relacionados à Bioquímica feitas pelos estudantes do curso de Fisioterapia durante a disciplina de Bioquímica do Depto de Bioquímica e Biologia Molecular.
A QUÍMICA DA VIDA
O texto a seguir foi retirado do início da parte 1 do livro de Bioquímica, do Voet. Trata de uma alusão perfeita ao significado da Bioquímic...
domingo, 1 de dezembro de 2019
ÁGUA, PH E SISTEMA TAMPÃO
ÁGUA
A
molécula de água, H2O, apresenta um caráter altamente polar devido
ao ângulo de 104,5 graus entre as duas ligações O-H. O seu átomo de oxigênio
possui 2 pares de elétrons livres, viabilizando a formação de pontes de hidrogênio
com moléculas vizinhas. Esta característica, faz com que ela possa se associe a
diversas substâncias, sendo chamada de solvente universal. Pode ser ionizada por
meio de uma reação ácido-base - caracterizada pela troca de prótons entre pares
conjugados de ácidos e bases - podendo se comportar como ácido e como base. Essas
são reações de equilíbrio, às quais correspondem constantes de equilíbrio
definidas pelo cálculo de “K”, que mede a afinidade relativa das bases, de cada
par ácido-base conjugados (AH/ A- e H3O+/ H2O),
por prótons.
Clique nos links para saber mais sobre a água:
PH
A
concentração hidrogeniônica [H+] e os valores de [H+]
para a maioria das soluções são tão baixos que passa a ser difícil compara-los.
Assim, na prática o valor mais usado é do pH, calculado por meio da seguinte
equação: pH = pK + log [A-]/[AH].
Clique no link para saber mais sobre a definição do pH:
SISTEMA TAMPÃO
Tampões são sistemas aquosos que tendem
a resistir a variações no seu pH quando pequenas quantidades de ácido (H+)
ou base (OH-) são adicionadas. Um sistema tampão consiste de um
ácido fraco - doa de prótons - e sua base conjugada - aceita prótons.
A adição de ácido forte ou base forte a uma solução aquosa de um ácido fraco, por
exemplo, ácido acético, causa pequenas variações de pH, se a
solução estiver a um pH próximo do pK do ácido. É esse comportamento que caracteriza um
tampão ácido-base.
CURIOSIDADE
Para sabem mais sobre as relaç~es entre água, sistema tampão e pela, confere esse artigo:
TESTE SEUS CONHECIMENTOS
(UTFPR) A
água apresenta inúmeras propriedades que são fundamentais para os seres vivos.
Qual, dentre as características a seguir relacionadas, é uma propriedade da
água de importância fundamental para os sistemas biológicos?
A) Possui baixo calor específico, pois
sua temperatura varia com muita facilidade.
B) Suas moléculas são formadas por hidrogênios de disposição espacial linear.
C) Seu ponto de ebulição é entre 0 e 100 °C.
D) É um solvente limitado, pois não é capaz de se misturar com muitas substâncias.
E) Possui alta capacidade térmica e é solvente de muitas substâncias.
B) Suas moléculas são formadas por hidrogênios de disposição espacial linear.
C) Seu ponto de ebulição é entre 0 e 100 °C.
D) É um solvente limitado, pois não é capaz de se misturar com muitas substâncias.
E) Possui alta capacidade térmica e é solvente de muitas substâncias.
Resposta:
A água é
considerada um solvente universal, devido à grande capacidade de dissolver uma
enorme quantidade de solutos. Seu ponto de fusão é de 0°C (à pressão de 1 atm)
e seu ponto de ebulição é de 100°C (à pressão de 1 atm). A molécula de água é
polar e possui geometria angular.
Resp.: E
Resp.: E
Autoras Gabriela Herman e Mylena O. Viana
Postado no dia 1 de dezembro às 23: 58
Síntese e Importância da melatonina
Resenha
A melatonina é um hormônio produzido pela glândula pineal, e que está relacionada
ao ciclo circadiano, regulando a fisiologia temporal biológica do nosso
organismo como o ciclo dia/noite, atividade/repouso, sono/vigília e entre
outros. Sua síntese inclui uma via neural complexa envolve as células
ganglionares da retina que se conectam aos pinealócitos. Utilizando o nervo
óptico, o núcleo supraquiasmático, o hipotálamo lateral e as fibras
pré-ganglionares na medula espinhal, que fazem sinapse com o gânglio cervical
superior, e estas através dos nervos simpáticos pós-ganglionares alcançam a
glândula pineal. Em condições naturais ocorre uma produção rítmica circadiana
de melatonina. A exposição a luminosidade (UV) é suficiente para suprimir a
síntese de melatonina. Bioquimicamente, a síntese de melatonina ocorre em
etapas, o triptofano sofre a ação da enzima triptofano hidroxilase (TPH) que o
transforma em 5-hidroxitriptofano que por sua vez sofre a ação da descarboxilase
que o transforma em serotonina, ou 5-hidroxitriptamina, esta então é
transformada em N-acetilserotonina pela enzima aril-alquil-n-acetiltransferase
(AANAT) que por fim sofre a ação da hidroxi-indol-oxi-metiltransferase (HIOMT)
que a transforma em melatonina (N-acetil-5-metoxitriptamina). A melatonina
também é sintetizada em outros órgãos do corpo humano, como na pele e trato
gastrointestinal, porém nesses casos ela não é liberada da corrente sanguínea
pois é usada localmente como antioxidante. A meia vida da melatonina na
corrente sanguínea em humanos é de aproximadamente 44 minutos. Uma vez na
corrente sanguínea ela é encaminhada ao fígado que a metaboliza e a transforma
em 6-sulfatoximelatonina que posteriormente é excretado na urina. A taxa de 6-sulfatoximelatonina
na urina é diretamente proporcional a síntese de melatonina, sendo um bom
indicador para exames não invasivos. Além de sua síntese diminuir com o
envelhecimento e sabe-se que pode estar relacionado a vários efeitos
fisiológicos dessa faixa etária. A melatonina é um hormônio bastante importante
para o ser humano, por seu famoso efeito regulador do nosso relógio biológico,
além dessa função ela também está relacionada como por exemplo no seu efeito oncostático,
sua interação com o sistema imune, gonadotrófico, seu potente efeito
antioxidante, o que lhe dá a
capacidade de recuperação de células epiteliais expostas
à radiação ultravioleta, sua modulação do sistema dopaminérico,
serotoninérgico, sua potencialização da analgesia opióide e da neurotransmissão
de GABA, sua implicação na produção de óxido nítrico e controle neurovascular. Além de ter a estrutura molecular semelhante à
indometacina, molécula de muito interesse na área das cefaléias. Atualmente, a
melatonina é altamente usada na indústria farmacêutica e em diversos
tratamentos como os dos distúrbios do sono, área estética
cefaléias, epilepsias e até mesmo na doença de Parkinson, onde em experimentos
foi observado que a melatonina melhora a qualidade do sono sem alterar
substancialmente as medidas de sono e sem alterar a função motora. Na sociedade
atual, onde a tecnologia está presente a cada segundo, o smartphone tem sido um
vilão, no quesito insônia, a tela do celular emite uma luz azul que sinaliza
para o sistema nervoso que ainda está dia, atrasando, diminuindo ou até mesmo
inibindo sua produção, levando a um uso excessivo de medicamentos para repor a
diminuição desse hormônio.
Referências:
Referências:
GENARIO,
Rafael. Efeitos da Melatonina sobre Doenças Neurodegenerativas: Um olhar prospectivo. 2016.
Disponível em:
<http://www.hcpf.com.br/ckfinder/userfiles/files/1%20Lugar%20Geral%20%20Rafael%20Genario%20-%20Efeitos%20da%20Melatonina%20sobre%20Doencas%20Neurodegenerativas%20um%20Olhar%20Prospectivo-1.pdf>.
Acesso em: 28 nov. 2019.
BRUIN,
Veralice
Meireles Sales de. IMPORTÂNCIA DA MELATONINA NA
REGULAÇÃO DO SONO E DO RITMO CIRCADIANO- UMA ABORDAGEM CLÍNICA. 2017.
Disponível em:
<http://www.sbpcnet.org.br/livro/57ra/programas/CONF_SIMP/textos/veralicebruin.htm>.
Acesso em: 26 nov. 2019.
PERES,
Mario Fernando Prieto. Melatonina e doenças
neurológicas. 2017. Disponível em:
<https://cefaleias.com.br/wp-content/uploads/2009/06/Melatoninaavan%C3%A7oseinstein.pdf>.
Acesso em: 28 nov. 2019.
SILVA
JUNIOR, José Sinersio
da. Os
efeitos do treinamento físico aeróbico sobre a síntese de melatonina pineal em ratossíntese
de melatonina. 2015. Disponível em:
<https://www.teses.usp.br/teses/disponiveis/42/42137/tde-19022016-152711/publico/JoseSinesiodaSilvaJunior_Mestrado_Corrigida_P.pdf>.
Acesso em: 26 nov. 2019.
https://drive.google.com/open?id=1GBIHJq6GNLUrjjiJonB8wOGCuzVInJ9R
Mapa Mental
https://drive.google.com/open?id=139F87UqtA9AMe1Z2KCb1XjsZT1d590vt
Artigo
OS
EFEITOS DO TREINAMENTO FÍSICO AERÓBIO SOBRE A SÍNTESE
DE
MELATONINA PINEAL EM RATOS (SILVA. 2015)
https://drive.google.com/open?id=1ueXPOM5VcGDvufbBMqgfcJn1w_Dg0rTyFelipe e Ayla (9)
Efeitos bioquímicos dos esteroides usados como suplemento
RESENHA SOBRE: Os efeitos bioquímicos dos esteroides usados como suplemento
Grupo 19, Caroline Bellani e Maria Eduarda Cubis.
Esteroides anabolizantes são derivados sintéticos do hormônio
testosterona que auxiliam no aumento da
musculatura, na perda de gordura e melhora do desempenho físico. Assim essa
droga passou a ser muito utilizada em academias como suplemento, uma pratica
arriscada do ponto de vista biológico, uma vez que será em grande parte
prejudicial. Além disso, existe grande alteração das variáveis bioquímicas. Os
efeitos hepatotóxicos incluem colestase (condição na qual a bile não pode fluir do
fígado ao duodeno), peliose hepática, hiperplasia nodular regenerativa,
neoplasia hepática e sangramento de varizes secundárias à hipertensão portal. A
intensidade dos resultados nocivos depende das características da exposição e
da suscetibilidade do usuário. A toxicidade desses produtos é observada principalmente
sobre os sistemas cardiovascular, hepático e neuroendócrino.
Após a ingestão o anabolizante sofrerá alterações para que seja
absorvido pelas células, dentro delas se ligará a um receptor androgênico para ser transportado a uma região no núcleo,
dependendo da estimulação dos receptores pode alterar o funcionamento de alguns
genes, fazendo as células produzirem proteínas. Esse mecanismo é compreendido
como a forma direta de metabolização dos esteroides. Diferentemente a maneira
indireta ocorre pela interação com fatores tróficos ou receptores de
glicocorticoides que inibem a degradação de proteínas. Independente do meio
como se apresenta, o objetivo final é aumentar a quantidade proteica citosólica,
afetando o ritmo de ativação de seu sistema enzimático. A associação do uso de
anabolizantes com a atividade física faz com que a célula aumente a produção de
receptores androgênicos no músculo.
Alguns efeitos proveitosos já foram encontrados com o
uso dos anabolizantes, porem são passageiros e pouco relevantes comparados aos
problemas que pode-se ter. As
miofibrilas aumentam em quantidade e volume devido ao edema ou pelo conteúdo
sarcoplasmático que se acumula, dando a impressão de ganho de força muscular.
Seguindo essa linha de raciocínio as mitocôndrias também são afetadas,
multiplicando-se e desta forma elevando a capacidade de respiração celular.
Foram estudados ainda o maior teor de nitrogênio no organismo e a quantidade
elevada de cortisona no sangue que de forma geral podem ser benéficos.
Dentre os efeitos mais graves da utilização
indiscriminada desse hormônio está a arteriosclerose que é a degeneração de
artérias devido à destruição das fibras musculares lisas e das fibras elásticas
que a constituem, levando a um endurecimento da parede arterial, geralmente
resultado de hipertensão (outro efeito colateral dos esteroides). Com a
ingestão dos anabolizantes, não existe mais necessidade de segregação da
quantidade normal de testosterona, assim os hormônios estimulante das células
intersticiais (ICSH) e o folículo estimulante ficam reduzidos quando existe
quantidade suficiente de testosterona. Como resultado, o testículo se atrofia e
ocorre a diminuição na contagem de espermatozoides. Entre as consequências
ainda está a ginecomastia é o desenvolvimento de tecido mamário no homem que
pode vir acompanhado de sensibilidade ao toque (pode voltar ao normal quando
interrompido o uso). Um estudos científico, utilizando voluntários que faziam
uso abusivo dessas drogas, comprovou a diferença bioquímica no organismo desses
indivíduos quando comparados a um grupo controle, através da avaliação de
plaquetas, eritrócitos, hemoglobina e enzimas hepáticas. Quanto aos hormônios
testosterona e estradiol houve um aumento significativo na circulação livre encontrada
nas amostras, assim como das enzimas hepáticas creatina quinase, aldolase,
transamina glutamil peroxidase e transamina glutamil oxidase, apresentou ainda
significativa alteração da concentração hormonal do eixo hipotálamo-hipófise-gonadal.
Quantitativamente as plaquetas também tiver expressivo aumento. O HDL foi o
único componente estudado que teve diminuição comparando ao grupo que não fazia
uso.
REFERENCIAS:
ABRAHIN, ODILON SALIM COSTA; SOUSA, EVITOM CORRÊA DE. Esteroides
anabolizantes androgênicos e seus efeitos colaterais: uma revisão
crítico-científica. Revista da Educação
Física / UEM. Vol.24 no.4 Maringá Oct./Dec. 2013.
DUTRA, BRÍGIDA SOUZA CÕRTES; et al. Esteroides
anabolizantes: uma abordagem teórica. Revista
Científicada Faculdade de Educação e Meio Ambiente. Jul-dez, 2012.
FARIA, PÃMELA POUOUBEL; et al. Avaliação de parâmetros
físicos e biológicos de ratos wistar após administração de decanoato de
nadrolona. Acta Biomédica Brasiliensia.
Volume 3, nº 2, Dezembro de 2012.
VENÃNCIO, DANIEL PAULINO; et al. Avaliação descritiva
sobre o uso de esteroides anabolizantes e seu efeito sobre as variáveis
bioquímicas e neuroendócrinas em indivíduos que praticam exercício resistido. Revista Brasileira de Medicina do Esporte. Vol.16
no.3 Niterói May/June 2010.
Uma forma interessante de ligar os esteróides a bioquímica é quanto a função anabolica, ja que os mesmos aumentam significativamente essa função. Mas você sabe o que é o anabolismo? É o processo de construção de complexos orgânicos; uma sucessão de reações químicas que constroem ou sintetizam moléculas provenientes de compostos menores; é necessário energia para que isso ocorra.O corpo humano, para crescer e se manter, precisa recorrer a nutrientes do meio externo. Esses nutrientes são quebrados para prover energia que as células utilizam para continuar suas reações químicas no organismo. Os produtos da quebra desses nutrientes são pequenas moléculas que as células podem utilizar para construir blocos de moléculas maiores – literalmente formando um novo material a partir dos produtos desses nutrientes.
A função do anabolismo é, de forma simplificada, construir moléculas estruturais e funcionais. O processo anabólico utiliza monômeros para construir polímeros; um polímero é um grande complexo molecular feito de muitas moléculas menores semelhantes umas às outras, os monômeros. Para construir novas proteínas (moléculas grandes e complexas; polímeros), células precisam de aminoácidos (moléculas simples; monômeros), os quais compõem as proteínas. As células obtêm esses aminoácidos absorvendo-os da corrente sanguínea e esse é considerado um processo anabólico; a construção de proteínas a partir de moléculas menores, os aminoácidos.
Bom, agora que você aprendeu um pouco sobre o anabolismo, entenda o efeito dos esteroides nesse processo por meio do artigo abaixo!
A função do anabolismo é, de forma simplificada, construir moléculas estruturais e funcionais. O processo anabólico utiliza monômeros para construir polímeros; um polímero é um grande complexo molecular feito de muitas moléculas menores semelhantes umas às outras, os monômeros. Para construir novas proteínas (moléculas grandes e complexas; polímeros), células precisam de aminoácidos (moléculas simples; monômeros), os quais compõem as proteínas. As células obtêm esses aminoácidos absorvendo-os da corrente sanguínea e esse é considerado um processo anabólico; a construção de proteínas a partir de moléculas menores, os aminoácidos.
Bom, agora que você aprendeu um pouco sobre o anabolismo, entenda o efeito dos esteroides nesse processo por meio do artigo abaixo!
ABRAHIN, ODILON SALIM COSTA; SOUSA, EVITOM CORRÊA DE. Esteroides
anabolizantes androgênicos e seus efeitos colaterais: uma revisão
crítico-científica. Revista da Educação
Física / UEM. Vol.24 no.4 Maringá Oct./Dec. 2013.
https://web.whatsapp.com/#
mapa mental https://mm.tt/1377856133?t=CjWlCp1oDQ
https://web.whatsapp.com/#
mapa mental https://mm.tt/1377856133?t=CjWlCp1oDQ
Efeitos bioquímicos dos esteroides usados como suplemento - artigo e correlação com a bioquímica
Uma forma interessante de ligar os esteróides a bioquímica é quanto a função anabolica, ja que os mesmos aumentam significativamente essa função. Mas você sabe o que é o anabolismo? É o processo de construção de complexos orgânicos; uma sucessão de reações químicas que constroem ou sintetizam moléculas provenientes de compostos menores; é necessário energia para que isso ocorra.O corpo humano, para crescer e se manter, precisa recorrer a nutrientes do meio externo. Esses nutrientes são quebrados para prover energia que as células utilizam para continuar suas reações químicas no organismo. Os produtos da quebra desses nutrientes são pequenas moléculas que as células podem utilizar para construir blocos de moléculas maiores – literalmente formando um novo material a partir dos produtos desses nutrientes.
A função do anabolismo é, de forma simplificada, construir moléculas estruturais e funcionais. O processo anabólico utiliza monômeros para construir polímeros; um polímero é um grande complexo molecular feito de muitas moléculas menores semelhantes umas às outras, os monômeros. Para construir novas proteínas (moléculas grandes e complexas; polímeros), células precisam de aminoácidos (moléculas simples; monômeros), os quais compõem as proteínas. As células obtêm esses aminoácidos absorvendo-os da corrente sanguínea e esse é considerado um processo anabólico; a construção de proteínas a partir de moléculas menores, os aminoácidos.
Bom, agora que você aprendeu um pouco sobre o anabolismo, entenda o efeito dos esteroides nesse processo por meio do artigo abaixo!
file:///C:/Users/Usuario/Downloads/1316-9067-1-PB.pdf
autoras: Caroline Bellani e Maria Eduarda Cubis (grupo 19)
A função do anabolismo é, de forma simplificada, construir moléculas estruturais e funcionais. O processo anabólico utiliza monômeros para construir polímeros; um polímero é um grande complexo molecular feito de muitas moléculas menores semelhantes umas às outras, os monômeros. Para construir novas proteínas (moléculas grandes e complexas; polímeros), células precisam de aminoácidos (moléculas simples; monômeros), os quais compõem as proteínas. As células obtêm esses aminoácidos absorvendo-os da corrente sanguínea e esse é considerado um processo anabólico; a construção de proteínas a partir de moléculas menores, os aminoácidos.
Bom, agora que você aprendeu um pouco sobre o anabolismo, entenda o efeito dos esteroides nesse processo por meio do artigo abaixo!
file:///C:/Users/Usuario/Downloads/1316-9067-1-PB.pdf
autoras: Caroline Bellani e Maria Eduarda Cubis (grupo 19)
METABOLISMO MUSCULAR
METABOLISMO MUSCULAR
O post de hoje está direcionado àquelas pessoas que já pararam enquanto estavam escrevendo e começaram a refletir sobre como os músculos estavam agindo para tornar aquela ação possível. Entenda este mecanismo complexo, porém incrível, do nosso corpo!
Se você já leu os nossos posts sobre metabolismo de carboidratos e regulação e integração de metabolismos, este aqui vai ficar um pouco mais simples de entender, então, antes de tudo, corre lá se você ainda não conferiu!
Como já comentado, as nossas células necessitam de energia para realizarem suas funções, e com as células musculares não é diferente. Para evitar que ocorra a fadiga muscular, e com elas todas aquelas dores que demoram para passar, os nossos músculos precisam ter moléculas energéticas disponíveis o tempo todo, dessa forma, diversas vias metabólicas atuam em conjunto tanto para armazenar energia para quando necessário, como também para a degradação destas no momento do exercício.
Saiba tudo sobre o metabolismo muscular pela vídeo aula abaixo:
https://www.youtube.com/watch?v=qbyD1toBdoo
Ainda está confuso? Assista a vídeo aula abaixo para esclarecer os pontos que deixaram restar dúvidas:
https://www.youtube.com/watch?v=CNaEWqwdsGY
Se você já leu os nossos posts sobre metabolismo de carboidratos e regulação e integração de metabolismos, este aqui vai ficar um pouco mais simples de entender, então, antes de tudo, corre lá se você ainda não conferiu!
Como já comentado, as nossas células necessitam de energia para realizarem suas funções, e com as células musculares não é diferente. Para evitar que ocorra a fadiga muscular, e com elas todas aquelas dores que demoram para passar, os nossos músculos precisam ter moléculas energéticas disponíveis o tempo todo, dessa forma, diversas vias metabólicas atuam em conjunto tanto para armazenar energia para quando necessário, como também para a degradação destas no momento do exercício.
Saiba tudo sobre o metabolismo muscular pela vídeo aula abaixo:
https://www.youtube.com/watch?v=qbyD1toBdoo
Ainda está confuso? Assista a vídeo aula abaixo para esclarecer os pontos que deixaram restar dúvidas:
https://www.youtube.com/watch?v=CNaEWqwdsGY
DISTROFIA MUSCULAR DE DUCHENNE
A distrofia muscular de Duchenne é uma doença genética degenerativa e incapacitante, caracterizada por degeneração progressiva dos músculos, devido a ausência ou deficiência da proteína distrofina na superfície das membranas musculares, o que afeta inclusive os músculos cardíacos e respiratórios, levando à morte.
O artigo intitulado "Distrofia muscular de Duchenne: complicações respiratórias e seu tratamento" de Fonseca et al (2007) dá um grande panorama sobre o que é esta doença e o que ela causa no organismo. Acesse o artigo pelo link abaixo:
CURIOSIDADE
Você sabia que para os seus músculos crescerem, é necessário que você danifique as células já existentes nele? Se isto é novidade para você, Jeffrey Siegel em um vídeo da TED, explica de uma maneira super didática todo este mecanismo. Ficou interessado? Acesse o vídeo através do link abaixo:
QUIZ
(PUC – PR-2007) Analise as afirmações abaixo, relativas ao processo do metabolismo energético:
I. Fermentação, respiração aeróbica e respiração anaeróbica são processos de degradação das moléculas orgânicas em compostos mais simples, liberando energia
II. Todos os processos de obtenção de energia ocorrem na presença do oxigênio.
III. A energia liberada nos processos do metabolismo energético é armazenada nas moléculas de ATP.
IV. No processo de fermentação, não existe uma cadeia de aceptores de hidrogênio que está presente na respiração aeróbica e anaeróbica.
V. Na respiração aeróbica, o último aceptor de hidrogênio é o oxigênio, enquanto na respiração anaeróbica é outra substância inorgânica.
VI. Na fermentação, a energia liberada nas reações de degradação é armazenada em 38 ATPs, enquanto na respiração aeróbica e anaeróbica é armazenada em 2 ATPs.
II. Todos os processos de obtenção de energia ocorrem na presença do oxigênio.
III. A energia liberada nos processos do metabolismo energético é armazenada nas moléculas de ATP.
IV. No processo de fermentação, não existe uma cadeia de aceptores de hidrogênio que está presente na respiração aeróbica e anaeróbica.
V. Na respiração aeróbica, o último aceptor de hidrogênio é o oxigênio, enquanto na respiração anaeróbica é outra substância inorgânica.
VI. Na fermentação, a energia liberada nas reações de degradação é armazenada em 38 ATPs, enquanto na respiração aeróbica e anaeróbica é armazenada em 2 ATPs.
Estão corretas:
a) I , III , IV , V
b) I , III , V , VI
c) I , IV , V , VI
d) I , II , IV , V
e) I , II , III, IV
b) I , III , V , VI
c) I , IV , V , VI
d) I , II , IV , V
e) I , II , III, IV
(RESPOSTA: A)
Autoras Gabriela Herman e Mylena O. Viana
Postado no dia 1 de dezembro às 23: 50
RESPIRAÇÃO CELULAR
RESPIRAÇÃO CELULAR
A respiração celular é, sem dúvidas, um processo fantástico
e cuja beleza vai além daquilo que vemos em livros de biologia – ela está mais
presente em nossas vidas do que imaginamos! Ao analisar o processo em que uma molécula de glicose é gradualmente
decomposta em CO2 e H2O e alguns ATPs são produzidos, obervamos três principais
etapas: glicólise, ciclo de Krebs e fosforilação oxidativa.
Na glicólise, a glicose – com seis carbonos - é convertida
em duas moléculas de piruvato – cada uma com três carbonos, produzindo ATP e
convertendo NAD+ em NADH. Ao ser
oxidado, o piruvato se torna uma molécula - chamada acetil-CoA - com dois
carbonos e ligada à CoenzimaA, liberando CO2 e produzindo NADH. No ciclo de Krebs, essa acetil-CoA
passa por uma série de reações, produzindo, dentre outros , NADH e FADH2. Estes, depositam elétrons na cadeia
transportadora de elétrons.
Um pouco confuso, né? Para
entender com maior profundidade esse maravilhoso processo, clique no link
abaixo e assista o vídeo:
CURIOSIDADE
Curiosamente, a
degradação da glicose, ou seja, a glicólise pode acontecer sem oxigênio, no processo
chamado fermentação, mas as outras três etapas da respiração
celular requerem oxigênio para ocorrer. E, notavelmente, apenas a fosforilação
oxidativa usa oxigênio diretamente.
A fermentação é de grande importância desde a antiguidade, destacadamente na produção de vinho, cerveja e pão,
TESTE SEUS
CONHECIMENTOS
(PUC - RJ-2007) São processos biológicos relacionados diretamente
a transformações energéticas celulares:
a) respiração e fotossíntese.
b) digestão e excreção.
c) respiração e excreção.
d) fotossíntese e osmose.
e) digestão e osmose.
Resposta: A
Autoras Gabriela Herman e Mylena O. Viana
Postado no dia 1 de dezembro às 23: 38
CATABOLISMO DE PROTEÍNAS E CICLO DA URÉIA
METABOLISMO DE AMINOÁCIDOS
Como vimos no
nosso último post, as proteínas - constituídas de subunidades monoméricas
chamadas aminoácidos (AA) - não são estocadas ou armazenadas em nosso
organismo! Nos animais, os aminoácidos podem sofrer degradação oxidativa diante
de certas circunstâncias, nas quais os aminoácidos são “quebrados”, separando
seus grupos amino e os α-cetoácidos. Sequencialmente, o processo de metabolismo
de aminoácidos ocorre da seguinte forma:
URÉIA
A ureia produzida
é um composto neutro, altamente solúvel e costuma ser excretado pela urina. É o
principal produto de excreção do excesso de nitrogênio vindo do catabolismo dos
aminoácidos no ser humano. Quando há ingestão normal de proteínas, a ureia representa
80% dos produtos nitrogenados na urina, onde se encontra também ácido úrico,
creatinina, íons amônio e outras formas menores de compostos nitrogenados. A
síntese de ureia acontece no fígado por meio de reações do ciclo da ureia. Para entender melhor esse processo, clique nos links e assista os vídeos:
CURIOSIDADE
Já entendemos que nós, organismos vertebrados, excretamos ureia. Mas você sabia que vários peixes de água
doce e invertebrados excretam amônia? Essa substância é muito tóxica e solúvel, o que faz com que muita água tenha que ser
eliminada. Assim, esse tipo de excreta só acontece em animais que não tem tanta "dificuldade" em obter água, ou seja, animais aquáticos. Os animais
terrestres transformam amônia em ureia ou em ácido
úrico. que são muito menos tóxicos, podendo ser acumulados por algum tempo no corpo e excretadas muita perda de água pelo organismo.
TESTE
SEUS CONHECIMENTOS
Quando a ureia é
sintetizada no fígado, todos processos a seguir podem ocorrer/ocorrem, EXCETO:
a. O glutamato pode ser
sintetizado a partir de α-cetoglutarato, utilizando uma série de reações de
transaminação.
b. O aspartato pode ser
sintetizado a partir do oxalacetato e glutamato, utilizando aspartato
transaminase.
c. O glutamato pode ser
sintetizado utilizando a reação de glutamato desidrogenase se o ião amónio
estiver em excesso.
d. O glutamato pode estar fornecendo
íons de amônio livre se a concentração de íons de amônio livre for baixa.
Resposta: C
Autoras Gabriela Herman e Mylena O. Viana
Postado no dia 1 de dezembro às 22: 56
Respiração Celular
Respiração celular
Afinal, o que é a respiração celular? É basicamente a conversão de energia em ATP.
Esse processo é divido em principais etapas que são: Glicólise, Ciclo de Krebs e a cadeia
transportadora de elétrons ou também conhecia como cadeia respiratória. De modo
geral, a respiração celular irá ter a respiração aeróbica e anaeróbica. Na imagem abaixo, um
breve resumo sobre as etapas da respiração:
transportadora de elétrons ou também conhecia como cadeia respiratória. De modo
geral, a respiração celular irá ter a respiração aeróbica e anaeróbica. Na imagem abaixo, um
breve resumo sobre as etapas da respiração:
Fonte:Brasil Escola.
Neste momento, iremos destacar a primeira etapa da respiração, a Glicólise.
O que é Glicólise?
São varias reações retiradas da glicose (energia) que irá ser quebrada em duas moléculas
de três carbonos chamadas de piruvatos. Com isso, na respiração celular a Glicólise será a
primeira etapa, porém não necessitando de oxigênio.
de três carbonos chamadas de piruvatos. Com isso, na respiração celular a Glicólise será a
primeira etapa, porém não necessitando de oxigênio.
Qual lugar ela ocorre?
A glicólise vai ocorrer no citoplasma da célula podendo ser dividida em duas fases principais:
a fase de investimento de energia e a fase de rendimento de energia.
a fase de investimento de energia e a fase de rendimento de energia.
Mas para explicar essas duas fases principais, um vídeo de um grande professor que irá
auxiliar nos estudos.
auxiliar nos estudos.
Um esquema geral para entender melhor;
Fonte: Researchgate
E depois dessa grande aula, que tal exercitar um pouco?!
(UEM) Assinale a alternativa correta a respeito da respiração celular.
a) A glicólise consiste na conversão de glicose em ácido pirúvico.
b) O ciclo de Krebs consiste na conversão de ácido pirúvico em ácido láctico.
c) Na cadeia respiratória, ocorre o transporte de hidrogênio para formar ácido pirúvico.
d) No ciclo de Krebs, ocorrem o transporte de hidrogênio, de oxigênio molecular e a
produção de água.
produção de água.
e) Todo o processo de respiração celular ocorre dentro das mitocôndrias.
Alternativa “a”. Na glicólise, a glicose é convertida em duas moléculas de ácido pirúvico.
Curiosidade
O filme “O nome da Rosa”, conta a história de um veneno inibidor da via glicolítica, o
“Arsenato” que pode ser incorporado no lugar do fosfato no gliceraldeido-3 fosfato,
não formando o 1,3 bifosfoglicerato, irá deixar deixa de formar 2 ATP causando intoxicação.
Bom filme!
“Arsenato” que pode ser incorporado no lugar do fosfato no gliceraldeido-3 fosfato,
não formando o 1,3 bifosfoglicerato, irá deixar deixa de formar 2 ATP causando intoxicação.
Bom filme!
Bons estudos!
Autoras: Maria Gabriele e Maria Fernanda -Grupo n°13 Postado em: 09/11/2019
Enzimas
A manutenção da vida celular depende da continua ocorrência de um conjunto de reações químicas, que devem atender duas exigências fundamentais: precisam ser altamente especificas, de modo a gerar produtos definidos, e devem ocorrer a velocidades adequadas a fisiologia celular, uma ausência de produção ou remoção de metabólitos pode levar a condições patológicas.
As enzimas exercem papel fundamental nessa produção e remoção. Enzimas são catalizadoras de reações podendo aumentar as ordens de grandeza das reações que catalisam e, sendo elas altamente especificas acabam selecionando as reações possíveis.
Elas são classificadas de acordo com a reação que ela catalisa, ao todo são seis classes: Oxido-redutases, catalisam oxido reduções; transferases, fazem a transferência de grupos; Hidrolases, que fazem a hidrolise de um composto; Liases, adicionam grupos a duplas ligações ou os removem deixando a dupla ligação; Isomerase, fazendo a isomerização e; Ligases, que condensam duas moléculas associadas a hidrólise de uma ligação.
Aprofundando o estudo das enzimas
Para entendermos como as enzimas funcionam na pratica recomendamos que você assista a uma vídeo aula do canal do professor Dorival Filho, onde o mesmo faz uma abordagem bem didática e compreensível sobre o assunto
Agora que você já compreende os conceitos básicos e se aprofundou no estudo das enzimas vamos testar o que foi aprendido com algumas questões:
1) Sabemos que as enzimas possuem papel fundamental nas reações químicas que ocorrem em nosso corpo. Marque a alternativa que indica corretamente a função dessas substâncias orgânicas nas reações do nosso organismo.
a) As enzimas atuam retardando a velocidade de uma reação.
b) As enzimas atuam aumentando a velocidade de uma reação.
c) As enzimas não atuam na velocidade de uma reação.
d) As enzimas atuam apenas degradando substâncias.
“b”. As enzimas atuam aumentando a velocidade de uma reação e, por isso, são consideradas catalisadores biológicos.
2)Sabemos que cada enzima atua somente em determinadas reações biológicas, pois cada uma é muito específica. Observe o desenho a seguir e marque a alternativa que indica o nome do modelo utilizado para explicar o funcionamento enzimático.
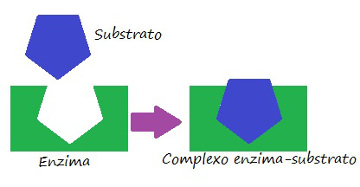
Observe o esquema exemplificando a especificidade da enzima

Observe o esquema exemplificando a especificidade da enzima
a) modelo do mosaico fluido.
b) modelo de encaixe.
c) modelo chave-fechadura.
d) modelo da porca-parafuso.
e) modelo ácido-base.
“c”. O modelo chave-fechadura é usado para explicar a especificidade da enzima, pois assim como apenas uma chave é capaz de abrir uma fechadura, a enzima atua apenas em reações específicas.
Autores: Dariel Matheus e Gustavo Raab (grupo 17)
Regulação hormonal do metabolismo
Muitas pessoas sabem que o metabolismo é uma série de reações químicas que permitem a funcionalidade dos seres vivos, mas ninguém presta muita atenção no processo de regulação dessas reações, que ocorrem afim de otimizar e disponibilizar os combustíveis e percursores metabólicos para cada órgão sem que haja desperdício.
Hormônios reguladores
Nos mamíferos o sistema neuroendócrino exerce uma função muito importante na coordenação do metabolismo dos órgãos. Temos alguns hormônios que são essenciais nessa regulação: Insulina, glucagon, adrenalina e cortisol.
A insulina é secretada pelo pâncreas em resposta a variação de glicose no sangue, sendo produzida pelas células beta pancreáticas. Seu objetivo é favorecer a variação do excesso de glicose em duas formas de armazenamento: no figado e músculo como glicogênio e no tecido adiposo como triacilgliceróis.
O glucagon é produzido pelas células alfa pancreáticas, sendo secretado quando há uma diminuição no índice de glicose sanguínea. Ele estimula a degradação do glicogênio, previne a glicólise e promove a gliconeogênese no figado, e ajuda na mobilização de ácidos graxos no tecido adiposo. O mesmo inibe a insulina.
A adrenalina é derivada da modificação da tirosina, secretada pelas glândulas suprarrenais. Sua função é sinalizar atividade eminente, tendo efeito de mobilização de combustíveis, inibindo o armazenamento dos mesmos.
O cortisol é produzido pelo córtex renal, sendo liberado mediante a ação de agentes estressores, como: ansiedade, medo, dor, hemorragia, baixa glicose sanguínea, infecção. Assim como a adrenalina, ajuda na mobilização de combustíveis.
Esse tema exige um maior aprofundamento para que haja uma real compreensão, vamos assistir uma vídeo aula da UNIVESP e nos situar no conteúdo: Estratégias de regulação do metabolismo
Curiosidade
A insulina é um hormônio importantíssimo para o nosso organismo e se faz presente na comum patologia que é o diabetes, mas falando especificamente do diabetes tipo 2, a qual o paciente apresenta resistência à insulina. É importante entender como se dá o processo de resistência insulínica. As causas da resistência insulina não são totalmente conhecidas, porém os estudos vêm mostrando que a principal alteração seria na sinalização celular referente aos transportadores de glicose (GLUTs). E outros estudos ainda relataram melhora na sinalização em resposta aos exercícios físicos modulando as proteínas inflamatórias que afetam a insulina.
fonte :
Autores: Dariel Matheus e Gustavo Raab (grupo 17)
MECANISMOS BIOQUÍMICOS DA TOXICIDADE DA AMÔNIA
Ao
estudar sobre os mecanismos bioquímicos da toxidade da amônia, observou-se que
o processo de catabolismo proteico tem como produto final a Amônia. Esse
composto na forma não ionizada é representado como NH₃ e na forma ionizada como NH₄⁺, compondo a amônia total (NH₄⁺ + NH₃). Como a forma não ionizada apresenta
uma grande capacidade de se difundir nas membranas celulares, conclui-se que é
o tipo mais tóxico de amônia. (CAMPOS et
al., 2012). Em condições normais, nos hepatócitos, o glutamato é transportado
até a mitocôndria pelo citosol, e nela sofre a desaminação oxidativa,
catalisada pela L-glutamato-desidrogenase. Em alguns processos do organismo é
gerada amônia livre através da degradação de nucleotídeos. Geralmente a amônia
livre é convertida em compostos não tóxicos antes de ser transportada para o
sangue e depois para fígado e rins. O glutamato é essencial para o metabolismo
do grupo amino, e é substituído pelo grupo l-glutamina. O glutamato se combina
com a amônia livre que foi produzida nos tecidos e então é produzida a
glutamina, pela ação da enzima glutamina sintetase (desempenha um papel
metabólico central). A glutamina transporta o amônio de uma maneira não tóxica.
(LEHNINGER, 2014). A toxicidade da amônia apresenta uma relação com o ciclo da
ureia, pois faz com que as reações iniciais desse ciclo ocorram dentro da
mitocôndria, para evitar que os íons amônia entrem em contato com a corrente
sanguínea. O excesso de amônia pode gerar uma grande utilização de
α-cetoglutarato (composto intermediário do Ciclo de Krebs) e diante disso,
gerar uma pequena disponibilidade desse composto para o CK, acarretando na
parada da cadeia transportadora de elétrons. (LEHNINGER, 2014). Para que a amônia
seja eliminada, ocorrem três etapas. A primeira delas, em que ocorre a remoção
de um grupo amino, é o processo de transaminação, em que o grupo α-amino é
transferido para o átomo de carbono α do α-cetoglutarato e produz o
α-cetoácido, semelhante ao aminoácido e ao glutamato. No segundo passo, há o
transporte de NH₄⁺
para o fígado, através de alanina e glutamina. E por fim, a eliminação de NH₄⁺ no fígado, através do ciclo da ureia. (LEHNINGER,
2014). Além do fígado, outro órgão importante para a excreção da ureia é o rim,
visto que quanto mais urina é produzida no rim, menor é a chance de
intoxicação. (KITAMURA, 2002). Para um bom funcionamento do ciclo da ureia, é
necessário que as enzimas carbamil fosfato sintase, ornitina transcarbamilase,
argininosuccinato sintetase, argininosuccinase e arginase estejam em atividade.
Além disso, é indispensável a presença dos substratos aspartato, arginina, ornitina, citrulina e
argininosuccinato, juntamente com três moléculas de ATP que foram geradas no
Ciclo de Krebs. (KITAMURA SS, 2002). A argina é a responsável pela excreção a
ureia e a partir dela é gerada a ornitina. “Na deficiência da Ornitina
Carbamoiltransferase, ou Ornitina Transcarbamilase (OTC), a função prejudicada
do ciclo da ureia resulta no acúmulo de níveis tóxicos de amônia no sangue e
cérebro, sendo os indivíduos mais gravemente afetados no início da vida”.
(SMITH et al., 2013) A deficiência dessa enzima afeta o funcionamento do ciclo
da ureia, elevando a amônia no sangue, juntamente com glutamina e alanina e
redução da citrulina plasmática (HERRAIZ GASTESI et al., 2015). Em condições
normais, nos hepatócitos, o glutamato é transportado até a mitocôndria pelo
citosol, e nela sofre a desaminação oxidativa, catalisada pela
L-glutamato-desidrogenase. Em alguns processos do organismo é gerada amônia
livre através da degradação de nucleotídeos. Geralmente a amônia livre é
convertida em compostos não tóxicos antes de ser transportada para o sangue e
depois para fígado e rins. O glutamato é essencial para o metabolismo do grupo
amino, e é substituído pelo grupo l-glutamina. O glutamato se combina com a
amônia livre que foi produzida nos tecidos e então é produzida a glutamina,
pela ação da enzima glutamina sintetase (desempenha um papel metabólico
central). A glutamina transporta o amônio de uma maneira não tóxica (LEHNINGER,
2014). Algumas patologias podem ser destacadas pelo aumento da glutamina e da amônia
na corrente sanguínea, afetando diretamente no cérebro (BATSHAW et
al., 2014). Uma delas é hiperamonemia que é a causa comum de encefalopatia
e dano cerebral irreversível em pessoas com a presença da deficiência da ornitina. (MACHADO;
FONSECA; JUKEMURA, 2013).
Alunas: Maria Fernanda
D. Medrades e Maria Gabriele A. Ramos – Grupo n° 13
REFERÊNCIAS
CARVALHO,
Layonne de Sousa. DOENÇA DA DEFICIÊNCIA DE ORNITINA CARBAMOILTRANSFERASE:
RELATO DE CASO INFANTIL. REVISTA UNINGÁ, v. 56, n. 4, p. 56-64, nov.
2019. ISSN 2318-0579. Disponível em: <http://revista.uninga.br/index.php/uninga/article/view/2902>.
Acesso em: 01 dez. 2019.
GUIMARÃES JÚNIOR, Roberto et al. O que é
ureia? Cadernos
Técnicos de Veterinária e Zootecnia, Belo Horizonte - Mg,
p.9-25, abr. 2016
KITAMURA, Sandra Satiko. Intoxicação por amônia em
bovinos e ratos: o desempenho real de desintoxicação e o emprego de tratamentos
alternativos. 2002. 117 f. Tese - Curso de Medicina Veterinária,
Universidade de São Paulo, São Paulo, 2002. Acesso em: 29. nov. 2019.
CAMPOS, Bruno Ribeiro de et al. TOXICIDADE
AGUDA DA AMÔNIA, NITRITO E NITRATO SOBRE OS JUVENIS DE CAMARÃO ROSA
FARFANTEPENAEUS BRASILIENSIS. Atlântica,
Rio Grande do Sul, p.75-81, 2012. Acesso em: 29. nov. 2019
Nelson, David L.; Cox, Michael M. Princípios
de Bioquímica de Lehninger - 6ª Ed. 2014. Editora Artmed. Acesso em: 01. dez. 2019
Um resumo sobre o assunto em forma de mapa conceitual:
Para acompanhar melhor a resenha, acesse nossos slides abaixo:
Para completar os estudos, sugerimos um artigo sobre a deficiência da ornitina carbamoil transferase, que gera uma doença grave. É muito interessante para observar os mecanismos de como a doença se desenvolve. Acesse o link abaixo para conhecer o artigo:
Assinar:
Comentários (Atom)
-
METABOLISMO DO ÁCIDO ARAQUIDÔNICO, SÍNTESE E FUNÇÃO DAS SUBSTÂNCIAS DERIVADAS A cascata do ácido araquidônico ( 20:4 [Δ⁵ ⁸ ¹¹ ¹⁴]) é u...
-
ÁGUA A molécula de água, H 2 O, apresenta um caráter altamente polar devido ao ângulo de 104,5 graus entre as duas ligações O-H. O seu...
-
Ao estudar sobre os mecanismos bioquímicos da toxidade da amônia, observou-se que o processo de catabolismo proteico tem como produto fi...





