 |
| Imagem: Produtora de vídeos Estúdio Ki |
Videoaula interessante!
O início da Bioquímica pode parecer um tanto assustador, mas hoje em dia temos um recurso incrível a ser usado ao nosso favor, a tecnologia. Vídeos explicativos para que você possa pausar e ir acompanhado com as suas próprias anotações feitas em aula é uma ferramenta muito proveitosa. Mas logo surge a dúvida “Qual fonte é realmente confiável?”. Para solucionar esse problema, a Universidade Estadual de Goiás através do Centro de Ensino de aprendizagem em Rede criou um canal no Youtube com videoaulas confiáveis. A respeito do tema Água, PH e tampões eles produziram o vídeo com o título “Biofísica- Água, Soluções e Sistema Tampão” que é bem completo e vale a pena assistir.
Agora que você já assistiu ao vídeo, nós separamos uma pergunta retirada a prova da UTFPR de 2008 para te ajudar a fixar ainda mais o conteúdo.
A água apresenta inúmeras propriedades que são fundamentais para os seres vivos. Qual, dentre as características a seguir relacionadas, é uma propriedade da água de importância fundamental para os sistemas biológicos?
Depois de uma videoaula e uma pergunta de vestibular que tal um filme e uma pipoca para relaxar? O filme de 2014, Á Deriva (Against the Sun) do diretor Brian Falk é baseado em fatos reais e retrata a dificuldade de três pilotos da marinha americana para sobreviver após caírem no oceano pacífico. Adivinha, eles estão sem água, reparem nos efeitos que a falta de água acarreta no funcionamento do organismo, a desidratação é um problema grave! Bom filme.
O início da Bioquímica pode parecer um tanto assustador, mas hoje em dia temos um recurso incrível a ser usado ao nosso favor, a tecnologia. Vídeos explicativos para que você possa pausar e ir acompanhado com as suas próprias anotações feitas em aula é uma ferramenta muito proveitosa. Mas logo surge a dúvida “Qual fonte é realmente confiável?”. Para solucionar esse problema, a Universidade Estadual de Goiás através do Centro de Ensino de aprendizagem em Rede criou um canal no Youtube com videoaulas confiáveis. A respeito do tema Água, PH e tampões eles produziram o vídeo com o título “Biofísica- Água, Soluções e Sistema Tampão” que é bem completo e vale a pena assistir.
 |
Imagem: Folha dirigida
|
Teste seus
conhecimentos!
Agora que você já assistiu ao vídeo, nós separamos uma pergunta retirada a prova da UTFPR de 2008 para te ajudar a fixar ainda mais o conteúdo.
A água apresenta inúmeras propriedades que são fundamentais para os seres vivos. Qual, dentre as características a seguir relacionadas, é uma propriedade da água de importância fundamental para os sistemas biológicos?
A) Possui baixo calor específico, pois sua temperatura varia com muita facilidade.
B) Suas moléculas são formadas por hidrogênios de disposição espacial linear.
C) Seu ponto de ebulição é entre 0 e 100 °C.
D) É um solvente limitado, pois não é capaz de se misturar com muitas substâncias.
E) Possui alta capacidade térmica e é solvente de muitas substâncias.
 |
| Imagem: Filmes Life |
Um ótimo filme!
Depois de uma videoaula e uma pergunta de vestibular que tal um filme e uma pipoca para relaxar? O filme de 2014, Á Deriva (Against the Sun) do diretor Brian Falk é baseado em fatos reais e retrata a dificuldade de três pilotos da marinha americana para sobreviver após caírem no oceano pacífico. Adivinha, eles estão sem água, reparem nos efeitos que a falta de água acarreta no funcionamento do organismo, a desidratação é um problema grave! Bom filme.
Autores: Andressa Mourão, Dayana Solek e Gabriele G. Ikier (Grupo 6).
Publicado em 06/11/2019 às 13:00.
Publicado em: 06/11/2019 as 14:30
E nada melhor do que um bom filme para relaxar, escolhemos um filme que retrata sobre a escassez de água e a importância dela no planeta. O filme “Mad Max: Estrada da fúria” (2016) retrata um cenário apocalíptico em que os seres humanos foram exterminados pelas guerras e somente alguns têm acesso a água, dirigido por George Miller. Após assisti-lo, você irá valorizar mais a existência dela e verá como a água é indispensável em nossas vidas.
O hormônio antidiurético ADH é um mecanismo de regulação da água, que controla a sede, excreção da água pelos rins e da perda da mesma por meio da evaporação.
Resposta e mais questões no link: www.vestibulandoweb.com.br
Autores: Ayla Colmenarez e Felipe V. França (Grupo 9)
Publicado em: 06/11/2019 as 17:49h
Segue vídeo-aula do professor Kennedy Ramos, sobre a água e suas características bioquímicas, para ajuda-lo em seus estudos!
Para auxilia-los na resolução de exercícios sobre o assunto, segue a vídeo-aula do canal Khan Academy Brasil sobre o calculo solução-tampão:
 Um grande exemplo do sistema tamponante está na respiração. O tampão bicarbonato é efetivo em pH próximo a 7,4 e envolve três equilíbrios reversíveis entre o dióxido de carbono nos pulmões e o bicarbonato no plasma sanguíneo. Esse tampão aberto é responsável por manter a homeostasia e a vida por meio da respiração!
Um grande exemplo do sistema tamponante está na respiração. O tampão bicarbonato é efetivo em pH próximo a 7,4 e envolve três equilíbrios reversíveis entre o dióxido de carbono nos pulmões e o bicarbonato no plasma sanguíneo. Esse tampão aberto é responsável por manter a homeostasia e a vida por meio da respiração!
Se você quiser saber mais sobre o controle do balanço ácido/base proveniente dos rins, assista este vídeo aula!
Publicado em 06/11/2019 às 13:00.
Água, pH e tampões biológicos
Substâncias ácidas e básicas (determinadas pelo pH), água, e soluções tampão são frequentemente utilizadas pelo nosso organismo para diversas reações. Mesmo estando presentes no nosso corpo você pode se perguntar: o que é tudo isso? Pensando nessa dúvida, trouxemos para vocês uma vídeoaula, muito completa, produzida pelas professoras Nadja C. de Souza Pinto e Maria Teresa Machini do Instituto de Química da Universidade de São Paulo (USP). Aproveitem esse material e por fim, testem seus conhecimentos adquiridos, respondendo a questão abaixo.
Link para acesso a vídeoaula: <https://www.youtube.com/watch?v=1qRWuIYxl2o>
- Questão retirada do vestibular da Universidade Federal da Bahia:
(UFBA-BA). A quantidade de água nas células e nos tecidos:
a) tende a diminuir com o aumento da idade
b) tende a aumentar com o aumento da idade
c) permanece constante com o aumento da idade
d) não tem qualquer relação com a idade
e) tem relação com a idade mas é a mesma em qualquer espécie
Gab: A
Agora para você se apaixonar mesmo pela matéria, achamos uma curiosidade que vai te deixar de queixo caído. A Revista Exame publicou 8 curiosidades sobre a água, e a número 6 era toda baseada na bioquímica. Leia abaixo:
Água pode te deixar velho mais rápido
Tomar água com pH (potencial de hidrogênio) menor que 7,4 pode acelerar o processo de envelhecimento. Quem defende essa ideia é o cardiologista e nutrólogo brasileiro Lair Ribeiro. Ele explica que o pH do nosso sangue é aproximadamente 7,4. Quando você consome alguma coisa de pH diferente disso, o corpo tem que trabalhar para equilibrar esse líquido.
“Para alcalinizar o sangue, o corpo tem que acidificar algum lugar – o coração, o cérebro ou algum outro tecido”, ele diz.
E explica: “Os bebês são básicos. Conforme vamos envelhecendo, nos tornamos mais ácidos”.
A conclusão é que, tomando uma água de pH menor que o do sangue, você acelera seu processo de envelhecimento. Para quem já esqueceu a aula de química, vale lembrar: pH igual a 7 é neutro.Abaixo disso (1, 2, 3, 5 etc) é considerado ácido. Já pH acima de 7 (7,5, 8, 9 etc) é básico ou alcalino.
No Brasil, somente algumas águas engarrafadas têm pH superior a 7,5, e a água da torneira gira em torno desse número. Então, não custa conferir o rótulo antes de comprar, né?
Autoras: Ana Luiza Fiebrantz (Grupo 10).Publicado em: 06/11/2019 as 14:30
Água, pH e Tampão
Todos falam que é importante beber água todos os dias e que a água é de extrema importância para a vida, mas você sabe o porquê?! Com base nas propriedades químicas e físicas desse composto, nós vamos te fornecer uma videoaula do Emmanuel Davi (logo no link abaixo) para que você entenda o porquê de a água ser fundamental. Além disso, para complementar seu aprendizado também trouxemos um vídeo sobre o Sistema Tampão que engloba o famoso pH e possui uma relação direta com a água e consequentemente com o nosso organismo.
Água:
Sistema Tampão:
Agora que você já assistiu as videoaulas sobre o tema, é hora de praticar e fixar o que aprendeu. Para isso, separamos um exercício do Centro de Seleção ao Ensino Superior de Pernambuco (CESESP-PE) para você. Se sentir alguma dificuldade você pode consultar o mapa mental básico que foi anexado junto a pergunta!
(CESESP-PE) São funções da água no citoplasma celular:
I - atuar como solvente da maioria das substâncias;
II - não atuar na manutenção do equilíbrio osmótico dos organismos em relação ao meio ambiente;
III - constituir o meio dispersante dos colóides celulares;
IV - participar das reações de hidrólise;
V - agir como ativador enzimático.
A alternativa que contém as funções verdadeiras é:
a) I, II, III.
b) III, IV, V.
c) I, III, IV.
d) V, II, III.
e) III, II, I.
Resposta correta: C.
Resposta correta: C.
 |
| (Fonte: Canal Hollywood.) |
E nada melhor do que um bom filme para relaxar, escolhemos um filme que retrata sobre a escassez de água e a importância dela no planeta. O filme “Mad Max: Estrada da fúria” (2016) retrata um cenário apocalíptico em que os seres humanos foram exterminados pelas guerras e somente alguns têm acesso a água, dirigido por George Miller. Após assisti-lo, você irá valorizar mais a existência dela e verá como a água é indispensável em nossas vidas.
Autoras: Juliana Wencel; Karina Freitas; Luiza Helena Gonçalves (Grupo nº 5).
Publicado em 07/11/2019 às 16:30h.
SANGUE, TAMPÃO E pH
Em um organismo saudável, o pH sanguíneo deve estar entre 7,35 e 7,45. A alteração desse valor pode trazer diversos malefícios para o corpo como a dor de cabeça, confusão e fraqueza.
O sistema Tampão é de enorme importância para evitar a alteração destes valores, mantendo a homeostase do organismo. O vídeo a seguir, feito pela Khan Academy, demonstra como esse sistema atua na manutenção de um pH normal.
Quiz
Após assistir ao vídeo, tente responder essa questão do vestibular da UFScar para testar seus conhecimentos:
(UFSCar-SP) O pH do sangue humano de um indivíduo saudável situa-se na faixa de 7,35 a 7,45. Para manter essa faixa de pH, o organismo utiliza vários tampões, sendo que o principal tampão do plasma sanguíneo consiste de ácido carbônico e íon bicarbonato. A concentração de íons bicarbonato é aproximadamente vinte vezes maior que a concentração de ácido carbônico, com a maior parte do ácido na forma de CO dissolvido. O equilíbrio químico desse tampão pode ser representado pela equação:
CO2(g) + H2O(l) ↔ H2CO3(aq) ↔ H+(aq) + HCO-3(aq)
Analise as afirmações seguintes:
I. Quando uma pequena quantidade de base entra em contato com uma solução-tampão, os íons hidróxido reagem com o ácido do tampão, não alterando praticamente o pH dessa solução.
II. Quando a concentração de íons bicarbonato no sangue aumenta, o pH também aumenta.
III. Quando a concentração de CO2 no sangue aumenta, o pH diminui.
São corretas as afirmações:
a) I, apenas.
b) II, apenas.
c) III, apenas.
d) I e II, apenas.
e) I, II e III.
*resposta no fim da página
Recomendação: Broken 🎥
O filme britânico Broken (Quebrado), do diretor Rufus Norris, estreou em 2012 e acompanha a vida de Emily Cunningham, uma jovem portadora de diabetes mellitus tipo 1, que tem sua vida transformada após presenciar um acontecimento inesperado entre seus vizinhos.
A diabetes mellitus tipo 1 possui como sintoma a acidez do sangue, e por consequência a queda pH, que é mais baixo que o normal. O longa-metragem é uma ótima forma de se acompanhar os desafios de uma pessoas com essa doença.
Por isso deixamos essa recomendação!
Imagem divulgação de “Broken”
*resposta do quiz: E
Autora: Andressa Marochi (Grupo 11)
Publicado em 07/11/2019 às 22:00
Publicado em 07/11/2019 às 22:00
Água, pH e Tampão
Hoje iremos indicar uma aula de bioquímica para estudantes
do ensino superior, sobre Água, pH e Tampões. No link abaixo você encontrará
uma aula do Professor Reinan de Oliveira da Universidade Estadual de Goiás.
Alguns tópicos importantes como: propriedades físico/químicas da água, pH na
acidez ou basicidade de uma solução e ainda o controle desse pH serão
discutidos nessa aula.
Separamos também uma
questão que pode te ajudar nos estudos.
(UEL-PR) As soluções
tampão desempenham um papel importante em muitos processos químicos e
biológicos. Por exemplo, o plasma sanguíneo é uma solução tampão eficiente em
um meio no qual uma variação maior que 0,2 unidade de pH pode ocasionar a
morte. Considere as afirmativas a seguir.
I. A dissolução do ácido em água para a preparação de uma
solução tampão apresenta a constante de ionização igual a 1.
II. Um exemplo de solução tampão é aquela que contém uma
base fraca e um sal derivado dessa base fraca.
III. Adicionando-se quantidades molares semelhantes de ácido
acético e de acetato de sódio à água, obtém-se uma solução tampão.
IV. A solução tampão resiste às variações de pH, quando se
adicionam pequenas quantidades de um ácido ou de uma base.
Assinale a alternativa correta.
a) Somente as afirmativas I e II são corretas.
b) Somente as afirmativas I e IV são corretas.
c) Somente as afirmativas III e IV são corretas.
d) Somente as afirmativas I, II e III são corretas.
e) Somente as afirmativas II, III e IV são corretas.
Para você que gosta de série indicamos The Rain, uma
história cheia de ação sobre a chuva ácida que acabou com grande parte da
população do planeta.
Autora Maria Eduarda Cubis (grupo nº
19)
Propriedades da água e o hormônio antidiurético ADH
A água é um componente químico que garante que a vida humana exista, visto que ela é o composto mais predominante nos seres vivos, ela é o produto ou reagente de muitas reações metabólicas. A mesma possui propriedades fundamentais para a manutenção da vida. Uma delas seria a capacidade de solvatação de muitas moléculas orgânicas e inorgânicas.
A água possui uma capacidade de interação muito grande, isso é resultado da sua estrutura dipolar, que permite grande formação de pontes de hidrogênio. Ao se interagir com uma biomolécula ela pode mudar a sua estrutura e também a estrutura da biomolécula, possui um processo adaptativo químico excepcional.
 |
| Moléculas de água - Hype Science |
Essa molécula consegue se dissociar em íons hidróxido e prótons. A quantidade de prótons estará ligada com a escala logarítmica do pH. Nesse caso existe o tampão de bicarbonato agindo no equilíbrio do pH do líquido extracelular 7,35 e 7,45.
As causas de acidose (pH sanguíneo 7,35) incluem a cetose diabética e a acidose lática. A alcalose (pH 7,45) pode suceder ao vômito do conteúdo gástrico ácido. (Peter J. Kennelly, Ph.D. e Victor W. Rodwell, Ph.D)
O hormônio antidiurético ADH é um mecanismo de regulação da água, que controla a sede, excreção da água pelos rins e da perda da mesma por meio da evaporação.
O diabetes insípido nefrogênico, que envolve a incapacidade de concentrar a urina ou o ajuste a alterações sutis na osmolaridade do líquido extracelular, resulta da falta de responsividade dos osmorreceptores tubulares renais ao ADH. (Peter J. Kennelly, Ph.D. e Victor W. Rodwell, Ph.D)
Postagem realizada pela aluna Kethelyn Domingues Terra (2)
Água, pH e Tampão
Olá, se você está aqui é porque com certeza, tem alguma curiosidade a respeito deste tema ou precisa estudar para alguma prova. Não se desespere, iremos te ajudar!
Você já deve ter ouvido algo sobre a água por aí, mas, você sabe o que é ela, quimicamente falando? E qual sua importância para a vida e por que bebemos água?
Primeiramente, a água é o maior solvente que existe e é de extrema importância para manter a vida no organismo. Por que? Todos os indivíduos possuem água na sua constituição e graças as suas propriedades, podem acontecer as reações bioquímicas. Ela é encontrada de forma abundante no planeta terra, porém, não a sintetizamos. Dessa forma obtemo-las através da dieta. Dentre suas propriedades, destacamos o pH e tampão, mas o que é isso? O pH, ou potencial de Hidrogênio, é que define se a água, ou qualquer liquido, será ácido(< 7) ou básico(> 7). Já o tampão é uma solução aquosa em que quando adicionado alguma quantidade de ácido ou base o pH não muda ou sua mudança não é significativa.
Para entender melhor o tema, trouxemos alguns vídeos e perguntas.
1 1. A estrutura da molécula de água
2. pH e solução tampão
Questões
(Pism – UFJF/2014) A maior parte dos seres vivos é constituída por água, responsável por 70 a 85% de sua massa. Considere as afirmativas abaixo relacionadas às propriedades físico-químicas da água.
I) A molécula de água é polarizada, ou seja, apesar de ter carga elétrica total igual a zero, possui carga elétrica parcial negativa na região do oxigênio e carga elétrica parcial positiva na região de cada hidrogênio.
II) Na água em estado líquido, a atração entre moléculas vizinhas cria uma espécie de rede fluida, em contínuo rearranjo, com pontes de hidrogênio se formando e se rompendo a todo momento.
III) A tensão superficial está presente nas gotas de água, sendo responsável pela forma peculiar que elas possuem.
IV) O calor específico é definido como a quantidade de calor absorvida durante a vaporização de uma substância em seu ponto de ebulição.
Assinale a alternativa que contenha todas as afirmativas CORRETAS.
A) I e III
B) II e IV
C) I, II e III
D) I, II e IV
E) I, III e IV
Resposta e mais questões no link: www.vestibulandoweb.com.br
Hora da curiosidade
Você sabia que beber água demais pode matar?
Pois é, é verdade, beber água de forma exagerada, como por exemplo mais de 16 litros por dia, pode gerar uma “overdose” de água pois a partir dessa quantidade nosso corpo começa a acumular água gerando uma hiperidratação, isso leva a diminuição de sais fora das células, na tentativa do organismo consertar isso, acaba inchando as células, em neurônios, pode causar algumas perdas de funções, lesões, confusões mentais e até mesmo, a morte.
BRASIL, Scientific American. Água demais pode fazer mal e até matar. 2018. Disponível em: <http://sciam.uol.com.br/agua-demais-pode-fazer-mal-e-ate-matar/>. Acesso em: 05 nov. 2019.
Autores: Ayla Colmenarez e Felipe V. França (Grupo 9)
Água, pH e Tampões
E aí galera, na hora que bate o desespero para estudar o conteúdo de bioquímica, nada melhor que uma boa vídeo aula para retomar os conteúdos vistos em sala. Trouxemos para vocês uma aula sobre pH e tampões do canal "Química Simples" produzida por Vinícius Pavanelli e Arthur Guimarães, https://www.youtube.com/watch?v=lX0nCZrGfZw, relembrando que o conceito básico de sistema tampão é que ao ser adicionado uma quantidade de ácido ou base para uma solução, seu pH não sofre variação. Aproveitem o vídeo!
Para Fixar o Conteúdo
Para dar mais uma ajuda, trouxemos também um exercício sobre sistema tampão da Pontifícia Universidade Católica do Rio de Janeiro:
(PUCRJ) O tampão acetato pode ser preparado pela mistura, em solução, de acetato de sódio anidro (CH3COONa) e ácido acético (CH3COOH). O pH desse tampão pode variar de 4,0 a 5,4 de acordo com a proporção dessa mistura.
Sobre o tampão acetato, é ERRADO afirmar que:
a) o pH do tampão acetato depende da proporção entre o ácido acético e seu sal.
b) o pH da solução tampão nunca se altera após a adição de ácido forte.
c) o tampão acetato é característico da faixa ácida de pH.
d) o pH da solução tampão praticamente não se altera após a adição de pequena quantidade de água. e) a adição de NaOH ao tampão aumenta a concentração de acetato no meio.
(Gabarito: letra B)
(Gabarito: letra B)
Você Sabia?
Encontramos algumas curiosidades no site "MundoTRI" sobre como o pH equilibrado do corpo altera o seu desempenho para melhor no esporte.
- Para manter seu pH equilibrado, é necessário eliminar resíduos ácidos que são gerados através da ingestão de alimentos.
- Além dos diversos componentes existentes no corpo para auxiliar essa retirada de resíduos, entre eles estão os tampões químicos.
- Esses tampões são cálcio, fósforo, bicarbonatos associados ao transporte pela hemoglobina e ciclos de fosfatos.
Autoras: Giulia M. Guimarães e Kethelen Gonçalves (grupo 18)
Água, pH e Tampão
O pH (potencial de hidrogênio) foi definido por Sörensen como logaritmo negativo da concentração do íon de hidrogênio. Sendo pH = 7,0 neutro; pH < 7 ácido, sendo que quanto menor o numero do pH mais ácida é a solução; e quando o pH é > que 7 a solução é chamada de alcalina ou básica. Já o sistema de tampão é composto por ácidos e bases fracas e seus conjugados capazes de resistir uma alteração no pH após adição de base ou ácido forte.
Ainda com dúvidas? O canal Ensino MaisO2 explica a solução tampão de forma rápida e simplificada. Assista:
E agora, para exercitar o que você aprendeu responda:
1) Considere duas soluções aquosas (X e Y) de mesmo volume e de pH 2,0 e 4,0, respectivamente. Analise as afirmações a seguir:
I. A solução X é ácida.
II. A solução Y é básica.
III. A solução X é neutra.
III. A solução Y é neutra.
São afirmativas CORRETAS:
a) I e II apenas.
b) I e III apenas.
c) II e III apenas.
d) I, II e III.
e) I apenas.
Resposta correta: alternativa E
Dica de filme!
Blade Runner - O Caçador de Androides é um filme de ficção científica de 1982 que se passa em novembro de 2019 numa cidade futurista na cidade de Los Angeles, um local totalmente poluído por uma chuva ácida. Um ótimo filme para entender as consequências da mudança do pH da água.
Autor: Isabelle Almeida (grupo 12)
ÁGUA, PH E TAMPÕES
Quando o assunto é Bioquímica, nós sabemos que toda ajuda é bem-vinda. Pensando nisso, separamos para vocês alguns materiais para ajudar nos seus estudos sobre Água, pH e Tampões.
Começando do começo, a Água é uma substancia química dada pela formula H2O, sendo os dois átomos de hidrogênio ligados ao átomo de oxigênio por uma ligação covalente. Tais moléculas interagem entre si através da formação de pontes de hidrogênio, tal característica confere à água alta solubilidade e a fama de ser o solvente universal (para alguns gases e substancias orgânicas).
Segue vídeo-aula do professor Kennedy Ramos, sobre a água e suas características bioquímicas, para ajuda-lo em seus estudos!
Agora falando um pouco sobre pH e tampões, o Potencial Hidrogeniônico (comumente conhecido como pH) é determinado pela concentração de íons hidrogênio na solução e serve para medir o grau de acidez, neutralidade ou alcalinidade da mesma.
Para auxilia-los na resolução de exercícios sobre o assunto, segue a vídeo-aula do canal Khan Academy Brasil sobre o calculo solução-tampão:
Para ajudar na fixação do conteúdo, vamos fazer um exercício!
Quais das alternativas relatam características de uma solução tampão?
I- são soluções que resistem a alterações de pH.
II- as variações de pH que ocorrem em soluções tamponadas são tão radicais quanto em soluções não-tamponadas.
III- são utilizadas para manter constante o pH de um sistema e preparar soluções de pH definido.
(Resposta: I e III)
E para encerrar, uma curiosidade!
 Um grande exemplo do sistema tamponante está na respiração. O tampão bicarbonato é efetivo em pH próximo a 7,4 e envolve três equilíbrios reversíveis entre o dióxido de carbono nos pulmões e o bicarbonato no plasma sanguíneo. Esse tampão aberto é responsável por manter a homeostasia e a vida por meio da respiração!
Um grande exemplo do sistema tamponante está na respiração. O tampão bicarbonato é efetivo em pH próximo a 7,4 e envolve três equilíbrios reversíveis entre o dióxido de carbono nos pulmões e o bicarbonato no plasma sanguíneo. Esse tampão aberto é responsável por manter a homeostasia e a vida por meio da respiração!
Postado por: Alyssa Elias e Kelly de Paula, n.3
Publicado em: 15 de novembro de 2019, às 20:52
Água, pH e Tampões
A escala de pH é
usada para classificar as soluções de acordo com a acidez ou basicidade
(alcalinidade). A maioria dos organismos, incluindo os seres humanos, precisa
manter o pH dentro de uma faixa bastante estreita para sobreviver. Os tampões
biológicos, soluções que neutralizam as variações no pH,
são a chave para a estabilidade da concentração de íons nos sistemas biológicos.
Neste artigo da Khan Academy temos uma explicação bem detalhada sobre Água, pH
e Tampões.
QUIZ (UFSCar-SP) O pH do sangue humano de um indivíduo
saudável situa-se na faixa de 7,35 a 7,45. Para manter essa faixa de pH, o
organismo utiliza vários tampões, sendo que o principal tampão do plasma
sanguíneo consiste de ácido carbônico e íon bicarbonato. A concentração de íons
bicarbonato é aproximadamente vinte vezes maior que a concentração de ácido carbônico,
com a maior parte do ácido na forma de CO dissolvido. O equilíbrio químico
desse tampão pode ser representado pela equação:
CO2(g) + H2O(l) ↔ H2CO3(aq) ↔ H+(aq) + HCO-3(aq)
Analise as afirmações seguintes:
I. Quando uma pequena quantidade de base entra em
contato com uma solução-tampão, os íons hidróxido reagem com o ácido do tampão,
não alterando praticamente o pH dessa solução.
II. Quando a concentração de íons bicarbonato no
sangue aumenta, o pH também aumenta.
III. Quando a concentração de CO2 no sangue aumenta, o pH diminui.
São corretas as afirmações:
a) I, apenas.
b) II, apenas.
c) III, apenas.
d) I e II, apenas.
e) I, II e III.
Curiosidade!
Você sabia que o ph
do sangue pode ser muito importante para investigações de cenas de crime? O
reagente de Kastle-Meyer tem como objetivo identificar a presença de sangue em
quaisquer superfícies, utilizando-se de diversas substâncias químicas, tais
como a fenolftaleína, o peróxido de hidrogênio e o pó de zinco metálico. A
fenolftaleína, como indicador de pH, possui a propriedade de apresentar
coloração rosada em meio básico. Como o sangue é uma substância alcalina, se a
reação apresentar uma coloração rosada, há comprovação a existência de sangue
seco naquela superfície. No vídeo abaixo podemos ver como funciona a reação entre
o sangue e o reagente de Kastle-Meyer.
*a resposta correta do quis é a letra A
Autoras: Carolina Moreia, Anna Luiza Scherer e Amanda Santos (grupo 15)
Postado em 16/11/19 as 12:53
pH e tampão da Glutamina
Você sabia que o pH consiste em potencial hidrogeniônico que
indica a acidez, neutralidade ou alcanidade em uma solução aquosa?
E você sabia que a glutamina é essencial para o pH? Venha
ver a importância desta propriedade!
A glutamina faz o controle do balanço ácido/base para que o
pH sanguíneo varie apenas entre 7.35 e 7.45. A liberação de H+ ocorre quando há
a nutrição adequada dos rins. A maior produção de íons de hidrogênio (H+) é
quando existe maior produção de exercício físico, deste modo vão para os rins
onde ocorrerá a tamponagem da acidose. Quando os rins fazem a eliminação de
íons de H+, fornece amônia proveniente da glutamina. Porém quando o H+ está em excesso
só pode ser excretado com auxilio de um íon de amônia, onde pode ser excretado
com a urina.
Um bom tamponante de H+ é o bicarbonato. Quando acontece a
oxidação de carbonos da cadeia de glutamina, eleva a produção de bicarbonato
que vai para a corrente sanguínea onde irá tamponar os íons de H+.
TESTE SEUS CONHECIMENTOS
1- Sobre a o pH
da glutamina identifique as alternativas incorretas:
a)A glutamina faz com que o pH fique apenas em 7.45.
b)A tamponagem da acidose acontece nos rins.
c)Bicarbonato é um bom tamponante, que não ocorre quando há a oxidação de carbonos da cadeia de glutamina.
d)O H+ quando em excesso consegue ser excretado somente com a urina.
a)A glutamina faz com que o pH fique apenas em 7.45.
b)A tamponagem da acidose acontece nos rins.
c)Bicarbonato é um bom tamponante, que não ocorre quando há a oxidação de carbonos da cadeia de glutamina.
d)O H+ quando em excesso consegue ser excretado somente com a urina.
R: a, c
DOENÇA CAUSADA POR BAIXO TEOR DE pH
Fugindo um pouco do assunto de pH da glutationa, achei interessante abordar sobre a doença tireoidiana, que esta relacionada com o pH.
A glândula tireoide faz a absorção de iodo quando o pH está estável, desta forma quando o pH está baixo, podendo ser derivado de alimentos como o café, por exemplo. Deste modo níveis de pH baixo levam a doença tireoidiana.
Quer conhecer mais sobre esta glândula, que atua quando o seu pH está balanceado?
Saiba mais sobre a glândula tireoide
Autora: Anna Carolina dos Santos (grupo 1)
Publicado em 17/11/2019 as 10:40
"Beba água".
Quem nunca ouviu essa frase em uma situação de descontração em uma roda de amigos? Não dá para negar a relevância da água na nossa vida: no ambiente, na alimentação, na composição corporal e etc. Então, nota-se que a água é de extrema importância de todas as espécies.
 (fonte: Metrópolis)
(fonte: Metrópolis)
Quanto devo beber de água por dia?
Não há um valor fixo. Cada indivíduo tem um biotipo e um gasto energético, assim deve ser levado em consideração qual a atividade está sendo realizada no momento.
O único capaz de hidratar o corpo é a água. O suco, refrigerante e demais bebidas não são capazes de atuar na hidratação, visto que esses alimentos possuem nutrientes diversos e glicose. Então, quando ingeridos o corpo entende esses líquidos como "fontes de energia", logo, segue para a glicolíse.
A TV Arapuan (João Pessoa-PB) realizou uma reportagem mostrando a "hidratação no exercício físico" e a importância do consumo adequado de água.
Frisando o consumo adequado, há de ter um equilíbrio. O exagero também faz mal, assim como a escassez. MAS ATENÇÃO: Cuidado com a pedra no rim! Segue um vídeo do médico renomado Dráuzio Varella comentando sobre o assunto.
LEITURA INDICADA
O artigo de Reis e et al. com título "Efeitos agudos da ingestão de bebidas energéticas sobre os parâmetros hidro-eletrolítico durante exercício em esteira" traz uma discussão sobre a ingestão de bebidas energéticas pré-exercício e o nível de hidratação. Segue o link: http://ref.scielo.org/gz4zsy.
QUESTÃO PARA FIXAR
(ENEM/2007) Ao beber uma solução de glicose(C6H12O6), um corta-cana ingere uma substância:
a) que ao ser degradada pelo organismo, produz energia que pode ser usada para movimentar o corpo.
b) inflamável que, queimada pelo organismo, produz água para mandar a hidratação das células.
c) que eleva a taxa de açúcar no sangue e é armazenada na célula, o que restabelece o teor de oxigênio no organismo.
d) insolúvel em que água, o que aumenta a retenção de líquidos pelo organismo.
e) de sabor adocicado que, utilizada na respiração celular, fornece CO2 para manter estável a taxa de carbono na atmosfera.
Gabarito: A.
Postado por: Taisy Melo (Grupo 4).
Publicado em 17/11/2019 às 23:24.
Autores: Fernanda e Stephanie (grupo 8)
Publicado em: 18/11/2019 às 13:05
ÁGUA E EXERCÍCIO FÍSICO.
"Beba água".
Quem nunca ouviu essa frase em uma situação de descontração em uma roda de amigos? Não dá para negar a relevância da água na nossa vida: no ambiente, na alimentação, na composição corporal e etc. Então, nota-se que a água é de extrema importância de todas as espécies.

Quanto devo beber de água por dia?
Não há um valor fixo. Cada indivíduo tem um biotipo e um gasto energético, assim deve ser levado em consideração qual a atividade está sendo realizada no momento.
O único capaz de hidratar o corpo é a água. O suco, refrigerante e demais bebidas não são capazes de atuar na hidratação, visto que esses alimentos possuem nutrientes diversos e glicose. Então, quando ingeridos o corpo entende esses líquidos como "fontes de energia", logo, segue para a glicolíse.
A TV Arapuan (João Pessoa-PB) realizou uma reportagem mostrando a "hidratação no exercício físico" e a importância do consumo adequado de água.
Frisando o consumo adequado, há de ter um equilíbrio. O exagero também faz mal, assim como a escassez. MAS ATENÇÃO: Cuidado com a pedra no rim! Segue um vídeo do médico renomado Dráuzio Varella comentando sobre o assunto.
LEITURA INDICADA
O artigo de Reis e et al. com título "Efeitos agudos da ingestão de bebidas energéticas sobre os parâmetros hidro-eletrolítico durante exercício em esteira" traz uma discussão sobre a ingestão de bebidas energéticas pré-exercício e o nível de hidratação. Segue o link: http://ref.scielo.org/gz4zsy.
QUESTÃO PARA FIXAR
(ENEM/2007) Ao beber uma solução de glicose(C6H12O6), um corta-cana ingere uma substância:
a) que ao ser degradada pelo organismo, produz energia que pode ser usada para movimentar o corpo.
b) inflamável que, queimada pelo organismo, produz água para mandar a hidratação das células.
c) que eleva a taxa de açúcar no sangue e é armazenada na célula, o que restabelece o teor de oxigênio no organismo.
d) insolúvel em que água, o que aumenta a retenção de líquidos pelo organismo.
e) de sabor adocicado que, utilizada na respiração celular, fornece CO2 para manter estável a taxa de carbono na atmosfera.
Gabarito: A.
Postado por: Taisy Melo (Grupo 4).
Publicado em 17/11/2019 às 23:24.
Água, ph e solução tampão
A água é um dos
compostos químicos mais importantes e abundantes na terra, sendo o
solvente universal mais usado para dissolver solutos em uma solução.
Uma solução aquosa pode ter um ph ácido, neutro ou básico numa
escala de 0 (ácido) a 14 (básico), avaliar o ph é de grande
importância na manutenção de solos para cultivo, normalidade do ph
sanguíneo e afins. Para evitar alterações no ph é utilizado a
solução tampão, é uma mistura formada por um ácido ou base fraco, e
um sal desse ácido ou base.
- Para entender melhor a ligação entre água, ph e solução tampão e sua importância para o equilíbrio do ph do sangue, segue o vídeo abaixo:
- Para por em prática o que foi ensinado nessa postagem tente responder a pergunta:
(UFMG
2009) Considere
certa quantidade de água e suco de limão, misturados, contida em um
copo. Analise estas três afirmativas concernentes a esse sistema:
I.
O sistema é ácido.
II. O pH do sistema é maior que 7.
III. No sistema, a concentração dos íons H+ é maior que a dos OH–.
II. O pH do sistema é maior que 7.
III. No sistema, a concentração dos íons H+ é maior que a dos OH–.
A
partir dessa análise, é CORRETO afirmar que:
A) apenas as afirmativas I e II estão certas.
B) apenas as afirmativas I e III estão certas.
C) apenas as afirmativas II e III estão corretas
D) as três afirmativas estão corretas
Resposta: B
Publicado em: 18/11/2019 às 13:05
--------------------------------*******--------------------------------
- Água, pH e Tampões biológicos:
Bom dia pessoal, trouxe aqui uma ajuda extra sobre água, pH e tampões biológicos. Além de poder reforçar o conteúdo visto em aula, as vídeos aulas podem auxiliar para dúvidas que ficam pendentes ou ainda à aprender a matéria a partir de um ponto de vista diferente. Seguem abaixo 3 vídeos do canal Escola de Ciência da Vida, voltado ao ensino superior, trazendo a abordagem individual -por fim integrada, afinal os três assuntos tem correlação- de cada tópico. Espero que tirem proveito desse estudo
Sistema Tampão:
Tampões biológicos:
- Para fixação do conteúdo:
(UFRJ, 2014) Os tampões têm a propriedade de resistir a mudanças no pH. Isto ocorre porque essa soluções contêm um componente ácido e um básico em sua constituição. Um sistema tampão muito utilizado é o ácido acético/ acetato de sódio: CH3COOH(aq) → CH3COO– + H+ (aq). Dados que as concentrações iniciais do CH3COOH e CH3COO– são iguais e valem 0,125 mol/L, o pKa= 4,75, e que log de 0,98= 0,007, pode-se afirmar que:
A- a faixa de pH que este tampão tem eficiência máxima é 4,75
B- o pH da solução tampão é 6
C- para preparar 50 mL da solução de CH3COOH (0,125 mol/L) a partir de uma solução de 2,50 mol/L, o volume da solução concentrada a ser diluída é de 25,0 mL
D- a quantidade de água utilizada na preparação da solução tampão é muito importante, pois a razão [ácido]/ [base conjugada] depende do volume da solução
E- ao se adicionar 1,00 mL de HCl 1,00M à solução tampão, o pH final da solução é de 6
Resposta A (https://www.qconcursos.com/questoes-de-concursos/questoes/966b59da-c6)
- Você sabia?
Acidose (processo de diminuição do pH sanguíneo para menos de 7,35 -aumento de H+) é uma das causas de osteoporose. Quando se toma líquidos muito ácidos (refrigerantes por exemplo) cria-se uma situação metabólica no nosso corpo que estimula a perda óssea. No Japão, existem 2 hospitais que trabalham com água Funcional no Tratamento de Doenças. Esta água tem o pH considerado ideal que é o pH entre 9 e 10.
(https://www.acqualive.com.br/ph-da-agua)
Mariana Rodrigues (grupo 16)
--------------------------------*******--------------------------------
Vamos relembrar?
O que é uma solução Tampão?
''O conceito original de ação tamponante surgiu de estudos bioquímicos e da necessidade do controle do pH em diversos aspectos da pesquisa biológica, como por exemplo em estudos com enzimas que têm sua atividade catalítica muito sensível a variações de pH. Fernbach e Hubert, em seus estudos com a enzima amilase, descobriram que uma solução de ácido fosfórico parcialmente neutralizado agia como uma proteção contra mudanças abruptas na acidez e alcalinidade.”
Água, o que é?
Relembre os conceitos gerais
· Molécula composta: H2O;
· Polar: possui polo positivo e negativo;
· Solvente de muitas substâncias (universal);
· Tensão superficial: as moléculas de água próximas à superfície de um recipiente (ou em lagos) estabelecem maior número de ligações de hidrogênio, criando uma forte tensão entre elas. Tal fenômeno permite com insetos consigam ficar parados ou até caminhar sobre a lâmina de água;
· Classificação das substâncias quanto à solubilidade em água:
o Hidrofílica: substâncias solúveis;
o Hidrofóbicas: substâncias insolúveis.
· Participação da água em reações químicas:
o Reações de hidrólise: quebra com ajuda da água;
o Reações de síntese por desidratação: união com perda de água.
· Participa do transporte de substâncias;
· Atua como regulador térmico;
· Substância mais abundante nos seres vivos;
· Variações do teor de água nos seres vivos:
o Entre seres vivos;
o Entre tecidos ou órgãos do mesmo indivíduo;
o Entre faixas etárias diferentes.
O que é pH?
O pH corresponde ao potencial hidrogeniônico de uma solução. Ele é determinado pela concentração de íons de hidrogênio (H+) e serve para medir o grau de acidez, neutralidade ou alcalinidade de determinada solução.
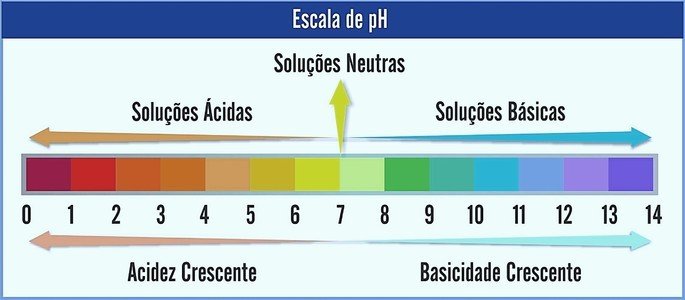
O pH é representado numa escala que varia de 0 a 14. Ela mede a acidez e basicidade de uma solução.
Sendo assim, o pH 7 representa uma solução neutra (por exemplo, a água pura). Já os que estão antes dele são consideradas soluções ácidas (pH ácido), e os que estão após o 7 são as soluções básicas (pH alcalino).
Feita essa observação, o caráter ácido é crescente da direita para a esquerda. Já o caráter básico, da esquerda para a direita. Note que, quanto menor o valor do pH mais ácida será a solução.
1. (Enem/2014) Um pesquisador percebe que o rótulo de um dos vidros em que guarda um concentrado de enzimas digestivas está ilegível. Ele não sabe qual enzima o vidro contém, mas desconfia que seja uma protease gástrica, que age no estômago digerindo proteínas.
Sabendo que a digestão no estômago é ácida e no intestino é básica, ele monta cinco tubos de ensaio com alimentos diferentes, adiciona o concentrado de enzimas em soluções com pH determinado e aguarda para ver se a enzima age em algum deles.
O tubo de ensaio em que a enzima deve agir para indicar que a hipótese do pesquisador está correta é aquele que contém:
a) cubo de batata em solução com pH = 9
b) pedaço de carne em solução com pH = 5
c) clara de ovo cozida em solução com pH = 9
d) porção de macarrão em solução com pH = 5
e) bolinha de manteiga em solução com pH = 9
b) pedaço de carne em solução com pH = 5
c) clara de ovo cozida em solução com pH = 9
d) porção de macarrão em solução com pH = 5
e) bolinha de manteiga em solução com pH = 9
Alternativa correta: b) pedaço de carne em solução com pH = 5.
A protease é uma enzima que digere proteínas e por ser gástrica ela age no estômago, cujo pH é ácido.
Analisando as alternativas, temos que:
a) ERRADA. A batata é rica em carboidrato e o pH do concentrado é básico.
b) CORRETA. A carne contém proteínas e as enzimas poderão agir nela, além do que o pH do concentrado é ácido, como o estômago.
c) ERRADA. O pH do concentrado é básico.
d) ERRADA. O macarrão é rico em carboidratos.
e) ERRADA. O pH do concentrado é básico.
PARA MAIORES DUVIDAS, DEIXO O LINK DE ALGUNS SITES QUE POSSUEM UMA DIDÁTICA MAIS ACESSIVEL E QUE PODE CONTRIBUIR PARA O NOSSO ENSINO!
Postagem realizada: Géssica, Tayala Erculano e Paulo (grupo 20).
------------------------------------------**------------------------------------------
ÁGUA, pH E SISTEMA TAMPÃO
Você já ouviu falar em chuva ácida? Este termo é usado para designar uma precipitação com pH inferior a 5.5, já que o pH normal da água da chuva é em torno de 5.6. Este fenômeno ocorre quando há alta concentração de gases como o dióxido de enxofre na atmosfera, pois eles reagem com gotículas de água, formando ácidos. Mas afinal, o que é pH? é uma escala numérica usada para classificar uma solução como ácida ou básica, a partir da quantidade de hidrônios que estão dispersos em tal solução. Quanto menor, o pH, mais ácida é a solução, e quanto menor, mais básica. Veja a escala abaixo
.jpg)
R: 1) mais ácido: vinagre
mais básico: café
2) alternativa E é falsa.
Para se divertir: Blade Runner – O Caçador de Androides – a ficção científica produzida em 1982 se passa na cidade de Los Angeles e o local está totalmente poluído por uma chuva ácida.
Autoras: Giovana Ribeiro e Luana Gonçalves (grupo 7)
Postado 28/11/2019 às 19:10
O pH do nosso organismo reflete diretamente em nossa saúde. O sangue humano possui um pH de 7,35 a 7,45 e caso esse valor varie, vários problemas serão desencadeados, pois com um sangue mais ácido, por exemplo, a ação do sistema imunológico é diminuída. Várias doenças, como osteoporose e problemas nos rins, também têm relação com o desequilíbrio do pH. Para evitar a variação do pH, nosso corpo possui um mecanismo denominado sistema tampão. Para entender melhor o que é um sistema tampão, sugerimos que assista a esta videoaula:
Principais tampões do nosso organismo: proteínas, fosfatos, íons bicarbonato.
Agora vamos testar os conhecimentos!
EXERCÍCIOS
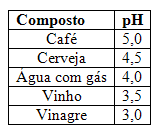
1) Os compostos abaixo estão relacionados em ordem crescente de acidez, diante desta dica, indique os materiais de menor e maior acidez.

2) (ESCS-DF) A tabela a seguir fornece a concentração hidrogeniônica ou hidroxiliônica a 25°C, em mol/L, de alguns produtos:
.jpg)
Com base nesses dados, NÃO é correto afirmar que:
a) a água do mar tem pOH = 6;
b) a água com gás tem pH maior do que a Coca-Cola e menor do que o leite de vaca;
c) a água do mar tem pH básico;
d) a clara de ovo é mais básica que o leite de vaca;
e) a clara de ovo tem maior pH do que a água do mar.
mais básico: café
2) alternativa E é falsa.
Para se divertir: Blade Runner – O Caçador de Androides – a ficção científica produzida em 1982 se passa na cidade de Los Angeles e o local está totalmente poluído por uma chuva ácida.
Autoras: Giovana Ribeiro e Luana Gonçalves (grupo 7)
Postado 28/11/2019 às 19:10
Água, pH e tampão
Nós sabemos a importância da água para o nosso cotidiano, mas agora vamos ver
a importância dela no nosso organismo. A água é o componente mais abundante
dentro das células, constituindo mais de 70% do peso delas. As moléculas se organizam
de acordo com a sua estrutura. Sabe-se que a maioria das reações bioquímicas ocorre
na água, que participa ativamente dessas reações. A geometria e as propriedades
dessa molécula como solvente são muito importantes para as propriedades dos seres vivos.
A fórmula da água apresenta dois hidrogênios ligados a um oxigênio, tem uma estrutura
tetraédrica e é uma molécula polar.
a importância dela no nosso organismo. A água é o componente mais abundante
dentro das células, constituindo mais de 70% do peso delas. As moléculas se organizam
de acordo com a sua estrutura. Sabe-se que a maioria das reações bioquímicas ocorre
na água, que participa ativamente dessas reações. A geometria e as propriedades
dessa molécula como solvente são muito importantes para as propriedades dos seres vivos.
A fórmula da água apresenta dois hidrogênios ligados a um oxigênio, tem uma estrutura
tetraédrica e é uma molécula polar.
Estrutura da molécula da água:
As soluções ácidas e básicas são classificadas dessa maneira pela concentração de íons
de hidrogênio em relação à agua pura. As soluções ácidas tem uma concentração de H⁺
maior do que a agua, já as soluções básicas tem uma concentração menor de H⁺.
Geralmente a concentração dos íons de H⁺ da solução é expressa em termos de pH.
Esse pH é calculado como o logaritmo negativo da concentração de íons de hidrogênio
de uma solução:
de hidrogênio em relação à agua pura. As soluções ácidas tem uma concentração de H⁺
maior do que a agua, já as soluções básicas tem uma concentração menor de H⁺.
Geralmente a concentração dos íons de H⁺ da solução é expressa em termos de pH.
Esse pH é calculado como o logaritmo negativo da concentração de íons de hidrogênio
de uma solução:
pH= - log10 [H⁺]
Ao colocar a concentração de íons de H⁺ da água, na equação acima, obtêm-se o valor de
pH=7, que é considerado o pH neutro.
pH=7, que é considerado o pH neutro.
Diante disso, foi criada uma escala para classificar as soluções de acordo com a acidez e
com a alcalinidade. A escala de pH varia de 0 a 14, sendo que 7 é neutro, abaixo de 7 é
acido e acima de 7 é básico ou alcalino. Escolhemos uma tabela para facilitar o seu estudo:
com a alcalinidade. A escala de pH varia de 0 a 14, sendo que 7 é neutro, abaixo de 7 é
acido e acima de 7 é básico ou alcalino. Escolhemos uma tabela para facilitar o seu estudo:
O pH das células humanas é em torno de 6,8 e do sangue é 7,4 , sendo muito próximos do
pH neutro. Os valores muito abaixo e muito acima de 7 são considerados prejudiciais a vida
humana. Porém, há regiões do organismo que suportam um pH bem menor, como o do
estomago, que é em torno de 1 e 2. Isso só é possível porque as células dessa região estão
constantemente morrendo e a região se renova rapidamente.
pH neutro. Os valores muito abaixo e muito acima de 7 são considerados prejudiciais a vida
humana. Porém, há regiões do organismo que suportam um pH bem menor, como o do
estomago, que é em torno de 1 e 2. Isso só é possível porque as células dessa região estão
constantemente morrendo e a região se renova rapidamente.
Os tampões biológicos tem a função de manter o pH ideal das células, neutralizando as
variações de pH. Quando houver muitos íons de H⁺ um tampão absorverá alguns deles
elevando o pH; quando houver poucos íons, um tampão doará alguns de seus H⁺ para
diminuir o pH.
Para que você consiga entender melhor o conteúdo, separamos uma vídeo aula bem
didática para te auxiliar:
variações de pH. Quando houver muitos íons de H⁺ um tampão absorverá alguns deles
elevando o pH; quando houver poucos íons, um tampão doará alguns de seus H⁺ para
diminuir o pH.
Para que você consiga entender melhor o conteúdo, separamos uma vídeo aula bem
didática para te auxiliar:
Agora que você já entendeu bem sobre o assunto, está preparado para responder uma
questão:
questão:
(UFSCar-SP) O pH do sangue humano de um indivíduo saudável situa-se na faixa de
7,35 a 7,45. Para manter essa faixa de pH, o organismo utiliza vários tampões, sendo
que o principal tampão do plasma sanguíneo consiste de ácido carbônico e íon bicarbonato.
A concentração de íons bicarbonato é aproximadamente vinte vezes maior que a
concentração de ácido carbônico, com a maior parte do ácido na forma de CO dissolvido.
O equilíbrio químico desse tampão pode ser representado pela equação:
7,35 a 7,45. Para manter essa faixa de pH, o organismo utiliza vários tampões, sendo
que o principal tampão do plasma sanguíneo consiste de ácido carbônico e íon bicarbonato.
A concentração de íons bicarbonato é aproximadamente vinte vezes maior que a
concentração de ácido carbônico, com a maior parte do ácido na forma de CO dissolvido.
O equilíbrio químico desse tampão pode ser representado pela equação:
CO2(g) + H2O(l) ↔ H2CO3(aq) ↔ H+(aq) + HCO-3(aq)
Analise as afirmações seguintes:
I. Quando uma pequena quantidade de base entra em contato com uma solução-tampão,
os íons hidróxido reagem com o ácido do tampão, não alterando praticamente o pH dessa
solução.
os íons hidróxido reagem com o ácido do tampão, não alterando praticamente o pH dessa
solução.
II. Quando a concentração de íons bicarbonato no sangue aumenta, o pH também aumenta.
III. Quando a concentração de CO2 no sangue aumenta, o pH diminui.
São corretas as afirmações:
a) I, apenas.
b) II, apenas.
c) III, apenas.
d) I e II, apenas.
e) I, II e III.
Resposta: Alternativa “E”
Todas são verdadeiras:
II. Quando a concentração de íons bicarbonato (HCO-3(aq)) no sangue aumenta, ocorre um
deslocamento do equilíbrio no sentido inverso para que esses íons sejam consumidos. Então
eles reagem com os íons H+, diminuindo a concentração deles no meio e aumentando o pH.
deslocamento do equilíbrio no sentido inverso para que esses íons sejam consumidos. Então
eles reagem com os íons H+, diminuindo a concentração deles no meio e aumentando o pH.
III. Quando a concentração de CO2 no sangue aumenta, ocorre um deslocamento do
equilíbrio no sentido direto para que o CO2 seja consumido. Então se forma, mais íons H+,
diminuindo o pH do meio.
equilíbrio no sentido direto para que o CO2 seja consumido. Então se forma, mais íons H+,
diminuindo o pH do meio.
Trouxemos como curiosidade o artigo “DISTÚRBIOS DO EQUILÍBRIO ÁCIDO-BÁSICO”
(Renato Marinho Furoni, et. al, 2010) que fala sobre distúrbios do equilíbrio ácido-básico,
discutindo alguns conceitos básicos de mecanismos de controle do pH sanguíneo.
De uma maneira didática, o texto tem como objetivo auxiliar no entendimento, diagnóstico e
condutas terapêuticas a serem realizados. Bons estudos e uma boa leitura!
(Renato Marinho Furoni, et. al, 2010) que fala sobre distúrbios do equilíbrio ácido-básico,
discutindo alguns conceitos básicos de mecanismos de controle do pH sanguíneo.
De uma maneira didática, o texto tem como objetivo auxiliar no entendimento, diagnóstico e
condutas terapêuticas a serem realizados. Bons estudos e uma boa leitura!
Autora: Maria Fernanda - Grupo n°13 - Postado em: 28/11/2019 ás 22:00
ÁGUA, pH e TAMPÃO
| Fonte: Google imagens |
A capacidade tamponante de uma solução também é considerada importante mais ou de igual significado do que o valor de pH que esta solução vai atuar. Foi realizado um experimento em uma disciplina de química sendo feito uma sequência de experimentos sendo trabalhados preparações de soluções, hidrólise e equilíbrios onde em um primeiro momento os alunos verificaram às cores desenvolvidas por meio de quatro indicadores crômicos em solução tampão que tinham pH variando de 3 a 11. Depois os alunos tiveram que fazer a titulação de uma solução tampão e por último os alunos tinham que preparar uma série de cores utilizando indicadores. No link abaixo você terá mais informações sobre como foi realizado o experimento
A MÁGICA DA ÁGUA QUE MUDA DE COR
Usando ingredientes que podem ser encontrados em um supermercado, foi possível realizar um experimento com um líquido roxo(retirado do repolho roxo) onde a partir desse líquido foi possível transformá-los em líquidos verde, azul, amarelo ou rosa. No link abaixo você verá como isto ocorre e os ingredientes utilizados.
QUIZ
(UFMG) Considere duas soluções aquosas diluídas, I e II, ambas de pH = 5,0. A solução I é um tampão e a solução II não.
Um béquer contém 100 mL da solução I e um segundo béquer contém 100 mL da solução II. A cada uma dessas soluções, adicionam-se 10 mL de NaOH aquoso concentrado.
Assinale a alternativa que apresenta corretamente as variações de pH das soluções I e II após a adição de NaOH (aq).
a) O pH de ambas irá aumentar e o pH de I será menor do que o de II.
b) O pH de ambas irá diminuir e o pH de I será maior do que o de II.
c) O pH de ambas irá aumentar e o pH de I será igual ao de II.
d) O pH de ambas irá diminuir e o pH de I será igual ao de II.
Alternativa “a”.
O pH de ambas as soluções aumentará (as soluções tendem a adquirir caráter básico), contudo, em razão do efeito tampão da solução I, a variação de pH nessa solução é menor do que na solução II, que não é tampão.
SUGESTÃO DE DOCUMENTÁRIO!!
| Fonte: Google imagens |
O documentário Bottled Life(“Vida Engarrafada”) é de caráter investigativo feito pelo jornalista Res Gehriger que elucida como a empresa suíça Nestlé tomou posse dos recursos hídricos em prol dos seus negócios.
Postado por Fernanda Vargas Lima (Grupo 21: Andressa K., Dalice A. e Fernanda Vargas







A recomendação do filme Broken foi muito bem feita.
ResponderExcluir